靶向蛋白降解嵌合体(PROTAC)以其事件驱动机制提高了药物疗效和选择性、拓展了药靶空间,成为新一代抗肿瘤药物治疗模式。然而,异源双功能分子嵌合体PROTAC分子量大、极性表面积高,导致其细胞透膜性差、口服生物利用度低,且所采用的泛素E3连接酶缺乏组织特异性,易引发“脱靶”系统性毒性,严重限制其临床转化。如何实现时空可控、低毒高效的精准靶蛋白降解,是PROTAC成药性优化的关键科学问题。

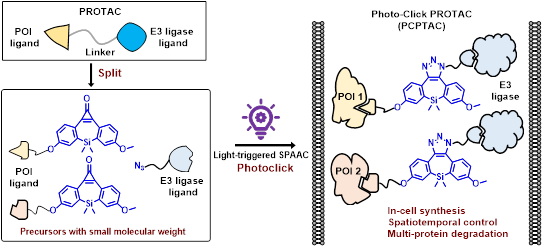
为此,龙亚秋教授课题组创新性提出“拆分-光点击(split-photoclick)”策略,将传统的大分子量PROTAC合理拆分为可光照偶联的两个小分子前体,创制了全新的光点击蛋白降解嵌合体(Photo-click Proteolysis-Targeting Chimera,简称PCPTAC)技术,实现活细胞内时空可控地原位合成多重PROTACs,达到协同抗癌疗效。相关成果发表于Angewandte Chemie International Edition。
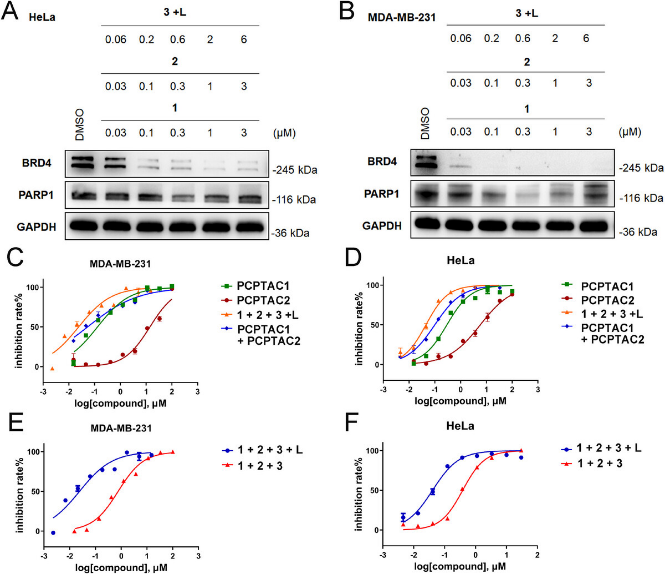
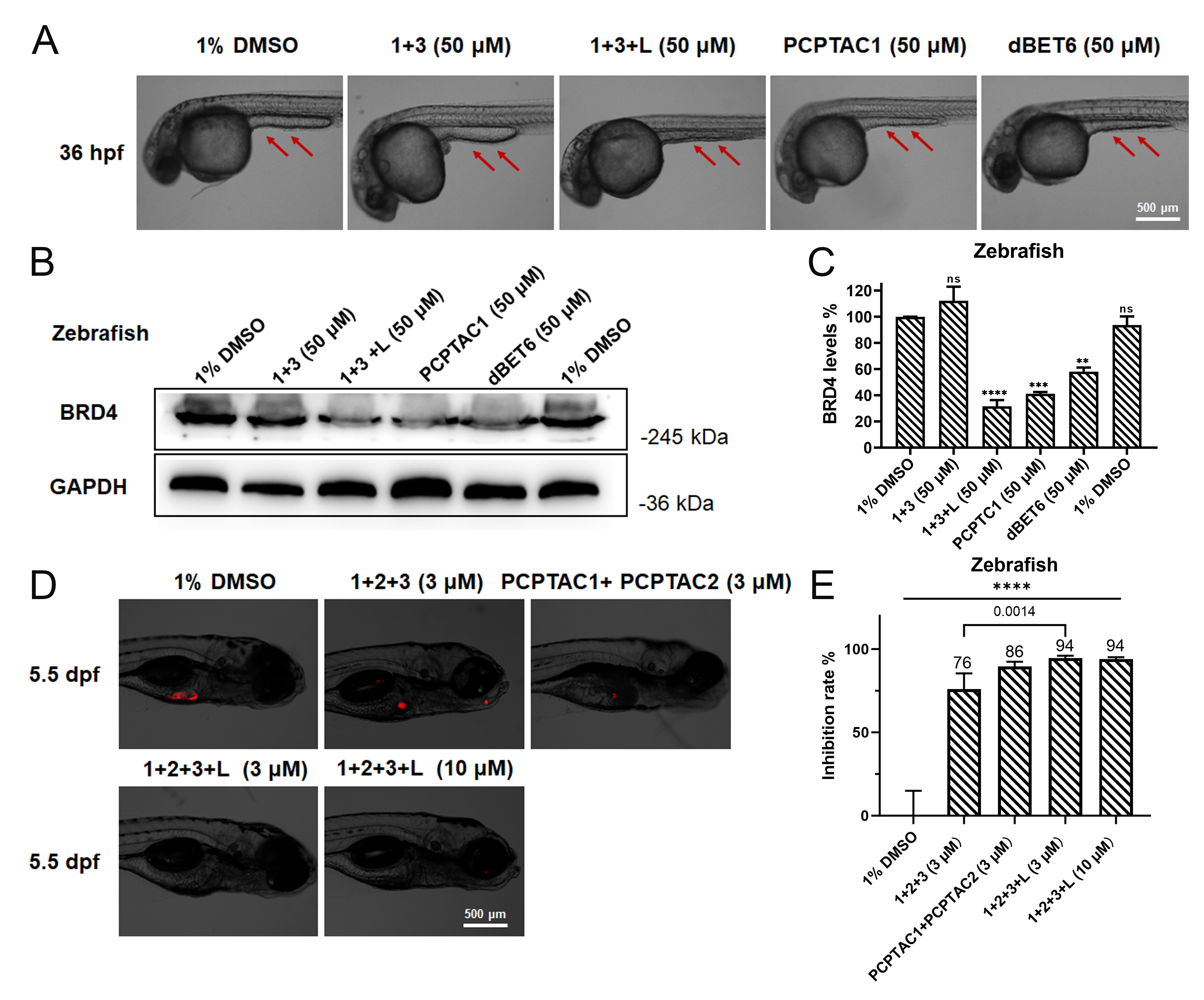
研究团队以具有合成致死效应的BRD4与PARP1两个致瘤蛋白为靶标进行概念验证,精心选取光笼蔽型二苯并硅杂环庚炔(photo-DBSH)分别与BRD4配体(+)-JQ1和PARP1配体Olaparib偶联,即合成得到photo-DBSH-JQ1(1) 和photo-DBSH-Olap(2),同时将互补的叠氮基团连接于E3泛素连接酶CRBN的配体泊马度胺上,即azide-Pomalidomide(3)。三者混合后光照,通过光引发的张力促进叠氮-炔烃环加成(SPAAC)反应在活细胞内快速高效合成双靶蛋白的PROTACs,实现一次光照多靶蛋白精准降解,并在细胞水平和斑马鱼动物模型上产生协同抑癌效果,活性均显著高于未光照前体组合和对应的传统PROTAC联用组。
该研究首次将光点击生物正交反应融入PROTAC创制了全新的PCPTAC技术,建立了模块化、普适性强的时空可控细胞内原位合成蛋白降解剂实现多重靶蛋白精准降解的平台:以“拆分”策略提升PROTAC嵌合体治疗模式的成药性;以“光点击”实现精准时空控制,提高靶向性和安全性;单次光照即可实现多靶同时降解,发挥协同抗肿瘤作用。PCPTAC技术为开发更安全、精准、高效的PROTAC药物提供了新范式。
论文信息
Jing Pang, Shihong Li, Yuhui Zhang, Qingyu Jia, Ya-Qiu Long*. Photo-click Proteolysis-Targeting Chimeras Enable Intracellular Generation of PROTACs for Precise Dual Protein Degradation.Angew. Chem. Int. Ed.2026,e18897, DOI: 10.1002/anie.202518897
团队与项目支持
本研究由苏州大学苏州医学院药学院博士后庞京博士作为第一作者完成,通讯作者为龙亚秋教授。研究得到国家自然科学基金、江苏省基础研究计划、江苏省卓越博士后计划、中国博士后科学基金等项目资助。